Trommers prov
Hej!
Hur får man reda på om provröret med olika sockerarter har en reversibel reaktion eller en irreversibel reaktion? Hur ska man även koppla reaktionsmekanism till detta?
Hej och välkommen till Pluggakuten!
Menar du hur du kan veta om kopparjonens reduktion är reversibel?
Ja precis det är det jag menar.
Utifrån den formeln:
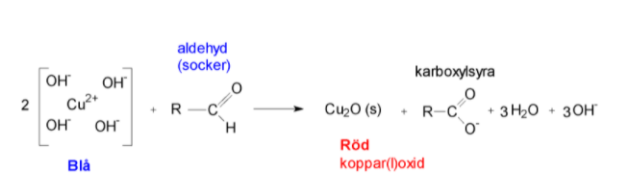
När kopparen har reducerats till Cu+ bildar den ett olösligt salt tillsammans med syre. Så reaktionen går inte tillbaka, då den ena reaktanten faller ur lösningen och då inte deltar i rekationen. Men i teorin kan den Cu+ överföra en elektron tillbaka till karboxylsyran.
Yes, tack så mycket.
Men kan det vara en reversibel reaktion eller irreversibel i Trommers prov? Eller kan det vara både. Jag undersökte glukos, sackaros och potatis mjöl.
De reaktionerna betraktas som icke-reversibla, av just den anledningen att ett olösligt salt bildas, så reaktionen kan inte "gå tillbaka". (Skulle reaktionsförhållandena i lösningen ändras kan nog reaktionen fås att gå baklänges, men det är inget man gör under Trommers prov - du vill ju kunna se om det finns reducerande kolhydrater i dina prover).
Tack så mycket, nu en annan fråga. Hur skulle detta kunna användas inom livsmedelskemi? Jag förstår inte denna frågan nu när det gäller uppgiften Trommers prov.
För all del!
Trommers prov används ju för att påvisa reducerade sockerarter, vilka är vanligt förekommande i livsmedel.
Kanske du kan fundera över hur detta kan användas för att följa kvalité, eller bestämma mängden av reducerande socker i ett livsmedel?
Aha oki, men hur har mängden reducerande sockerarter någon betydelse. Vad spelar det för roll?
En hel del (bio)kemi ingår i livsmedelsproduktion, och används där för att följa kemiska processer under tillverkningen. Och för att undersökt så att de producerade livsmedlen har en acceptabel kvalité, t.ex. att livsmedlet håller rätt kvalité och avviker från vad tillverkarna påstår om varan på förpackningen och dylikt.
Stärkelse t.ex. består av polymerer (långa kedjor) av glukosmolekyler, men endast änden av polymeren kan reducera kopparjonerna (för de reducerande ändarna hos resten av glukosmolekylerna är skyddade genom att de binder till andra glukosmolekyler). Så om stärkelsen bryts ner kommer mängden fria ändar öka, och med det kan fler kopparjoner reduceras.
Kolhydraten laktos i mjölk kan även reducera kopparjonerna. Vid syrning av mjölkprodukter omvandlas laktosen till laktat (mjölksyra) som sänker pH och får konsistensen att tjockna (som i filmjölk). Även vid tillverkning av mjuk och hårdost förbrukar mikroorganismer laktosen.
Finns det någon konsumentgrupp som är intresserade av att veta om mejeriprodukter innehåller laktos?
Ja, såklart de som är laktosintoleranta och jag förstår verkligen hur jag ska formulera den här frågan tackkk. Men om du har tid så har jag några frågor att fråga. Så som vad är reaktionsmekanismerna som ingår i laborationen? samt hur påverkar det vilken funktionell grupp de tillhör i Trommers prov?
Formeln för reaktionen kan du nog hitta på t.ex. engelska versionen av wikipedia.
Reaktionsmekanismen för reduktionen är nog något som dyker upp på universitetsnivån, snarare än Ke2, men bilden nedan visar reaktionen i mer detalj:

I korthet sker reduktionen i två steg, där varje steg reducerar en Cu2+ till Cu+.
samt hur påverkar det vilken funktionell grupp de tillhör i Trommers prov?
Jag förstår inte riktigt din fråga här, men provar ändå.
Redox-reaktionen som sker involverar aldehydgruppen, samt även om den angränsande kolatomen som hjälper till att skapa dubbelbindningen (motsvarande en keto-enol tautomerisation, men det är nog kemi på universitetsnivå snarare än Ke2).
Reaktionsmekanismen kräver mer kemikunskaper än Ke2, men om du vill kan vi prova att gå igenom även denna.
Ja snälla vill jättegärna du hade kunnat berättat det med reaktionsmekanismer i Trommers prov. Vill gärna förstå det.
Vi provar!

Steg 1: en bas (hydroxidjonen) tar en proton från kolatomen bredvid aldehyden, och bindningselektronerna som blir över bildar istället en dubbelbindning mellan kolen. Samtidigt flyttas bindningselektronerna i karbonylgruppen upp till syret (kolet kan inte ha fem bindningar, och denna omlagring av elektronerna löser detta problem). Detta är en “omlagring”, som kallas keno/enol tautomerisering (det bildas en enol, d.v.s. två kol förbundna med en dubbelbindning och med en hydroxigrupp på ett av kolen).
Steg 2: Ett elektronpar i enolens dubbelbindning börjar bilda en bindning till Cu2+ jonen (streckade linjen, elektronerna finns fortfarande i dubbelbindningen).
Steg 3: Ett av syrets fria elektronpar omlagras och återbildar dubbelbindningen till kolatomen, men nu kan inte enolens dubbelbindning ta upp en proton (för denna proton har hydroxidjonen försvunnit med), så istället skapas en bindning till kopparjonen som därmed får ta del av en elektron och reduceras till Cu+.
Steg 4: Karbonylkolet är öppet för en nukleofil attack från ännu en hydroxidjon, och för att detta skall gå omlagras ett elektronpar från dubbelbindningen till syret. Och resultatet är att en dialkohol bildas (två hydroxigrupper, varav den ena saknar sin proton), med Cu+ bundet.
Steg 5: Bindningen mellan kolet och kopparjonen bryts, och kopparjonen lämnar med en av kolhydratens elektroner. Så kvar på kolet är endast en elektron från elektronparet, d.v.s. en radikal bildas (markerat som den ensamma pricken, motsvarande elektronen). Radikaler är generellt tokreaktiva, så denna lämnar bums ifrån sig sin oparade elektron till en ny Cu2+ jon som reduceras till Cu+ (steg 6). Och istället bildas en karbokatjon bildas (markerat med plustecknet på kolet).
Steg 7: Elektronparet på syret omlagras och dubbelbindningen till kolet återskapas, samtidigt som en hydridjon (H-) flyttas till karbokatjonen (som då får sina önskade åtta bindningselektroner), och en proton (endast vätekärnan) försvinner då ytterligare en hydroxidjon tar denna.
Så till slut har vi en karboxylsyra istället!
Och detta går endast på detta vis när det finns massvis med hydroxdijoner som kan ta protoner och utföra den nukleofila attacken.

