Titreringskurva
Hej,
Jag har titrerat NaOH i HCL. Därefter skapat följande tabell:
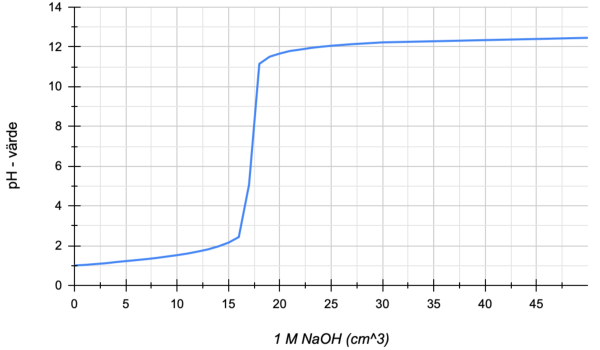 Jag förstår att ekvivalenspunkten är där vi har som mest lutning på vår tangent. Den brantaste lutningen vill jag påstå finns vid 5.75/6, men rätta mig gärna om jag har fel.
Jag förstår att ekvivalenspunkten är där vi har som mest lutning på vår tangent. Den brantaste lutningen vill jag påstå finns vid 5.75/6, men rätta mig gärna om jag har fel.
Jag tänker mig även att det måste finnas ett stökiometriskt sätt att utföra detta på? Det vill säga när jag har lika mycket bas som det från början fanns HCl. Jag har volym och koncentration HCl i bägaren, samt koncentration NaOH.
Dessutom tänker jag att det går att att göra det matematiskt utan stökiometrin. Om jag drar en trendlinje med viss funktion bör jag kunna hitta vid vilket pH värde min trendlinje korsar min ekvivalenspunkt. Men detta kanske är fel? Även inte möjligt att göra om man inte har den exakta volymen då neutralisationen sker.
mvh
Ekvivalenspunkten är vid v = 17,5 ml. Där ökar pH från 6 till 11 vid en mycket liten tillsats av NaOH. Om du vet volymen för HCl från början kan du beräkna den ursprungliga koncentrationen för saltsyran.
Eftersom varken natriumjoner eller kloridjoner har några syrabas-egenskaper är pH-värdet vid ekvivalenspunkten (d v s pH i NaCl-lösning) samma som för rent vatten, d v s 7.


