Tentafråga, reagenser
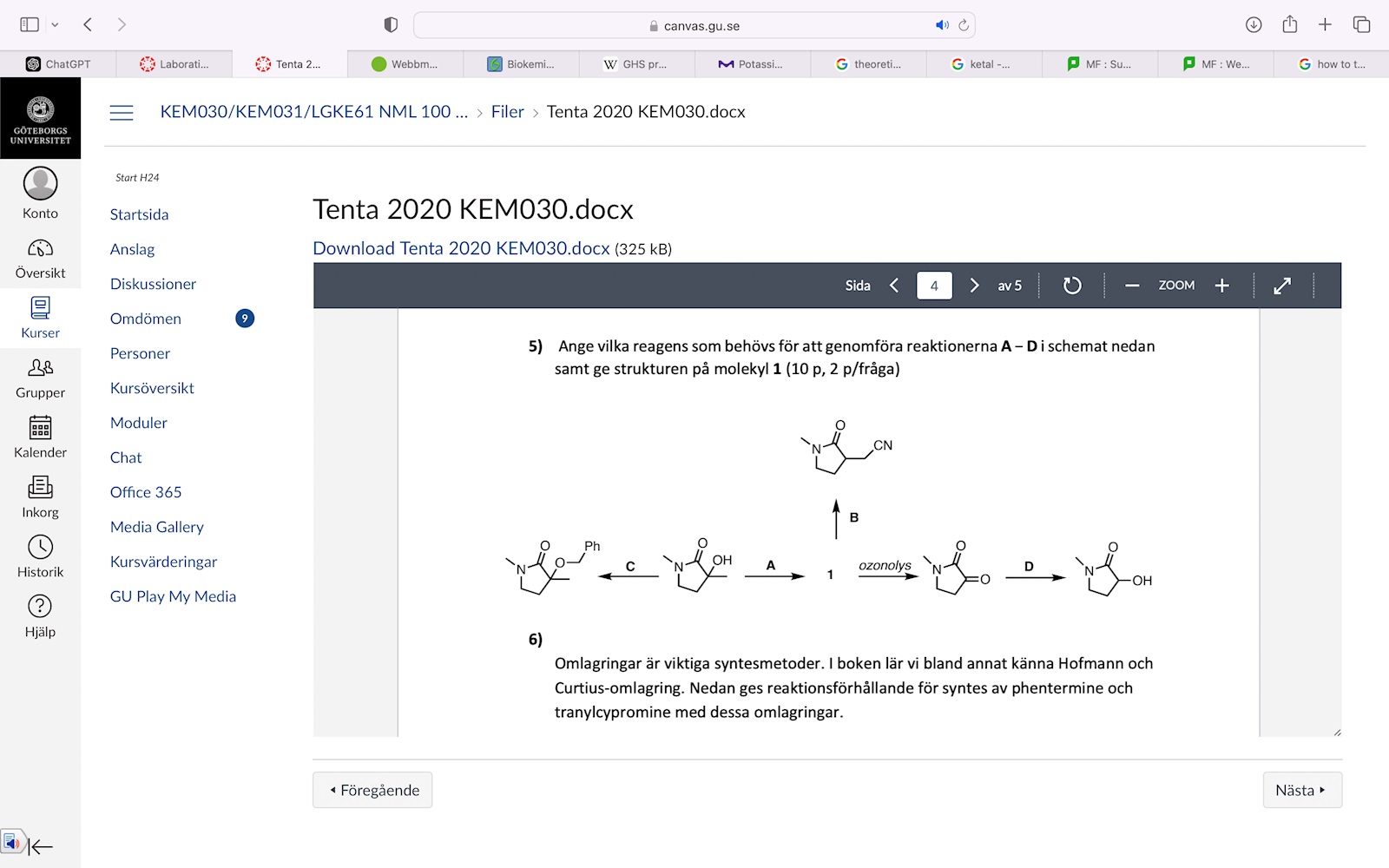
Här har vi en gammal tenta fråga.
Hur ska jag tänka för b? jag tänker att platsen med sifferan 1 är lik cyano-produkten, fast att metylen CN är bunden till istället är dubbelbunden till ringen. Dock vet jag inte en reagens där man kan göra en arken till en alkannitril. Några förslag?
För c tänker jag NaH + en bromofenyl.
För a tänker jag bas som NaOH för en E1cb reaktion. Då tänker jag mig att metylen bredvid hydroxylgruppen blir dubbelbunden.
För d tänker jag LiAlH4 + H3O.
Glarboo skrev:
Här har vi en gammal tenta fråga.
Hur ska jag tänka för b? jag tänker att platsen med sifferan 1 är lik cyano-produkten, fast att metylen CN är bunden till istället är dubbelbunden till ringen. Dock vet jag inte en reagens där man kan göra en arken till en alkannitril. Några förslag?
Om 1 innehåller en methinegrupp så kan du väl bara göra en hydrocyanering, och på så vis få cyano-produkten.
För c tänker jag NaH + en bromofenyl.
Bromofenyl fungerar inte, det blir ett kol för lite, du behöver (bromometyl)benzen i så fall.
Finns det inte en risk att hydriden angriper metylkolet, och substituerar brom så att du istället får etylbensen. Vet inte om du behöver specificera närmare hur reaktionen skall ske, temperatur lösningsmedel etcetera, men skillnader där kan nog användas för att styra reaktionen mot den produkt du önskar.
För a tänker jag bas som NaOH för en E1cb reaktion. Då tänker jag mig att metylen bredvid hydroxylgruppen blir dubbelbunden.
För en E1cb reaktion kräver en sur protonen på beta-kolet, och en ganska svag lämnande grupp på alfa-kolet. Och det finns ingen klassiskt sur proton att ta - den enda som ligger i närheten är en på metylgruppen, och anjonen som skulle bildas på metylkolet kan inte stabiliseras någon stans.
Men att abstrahera protonen på metylgruppen genom en bas är en bra tanke, på så vis kan elektronparet i bindningen C-H omlagras till C=C och hydroxidjonen lämna. Men NaOH riskerar väl även att abstrahera hydroxigruppens proton?
För d tänker jag LiAlH4 + H3O.
Jo det borde fungera.

