Reduktion av NAD+
Hej,
jag har lite problem att förstå reduktionen av NAD+ till NADH där reaktionsformeln är som följer: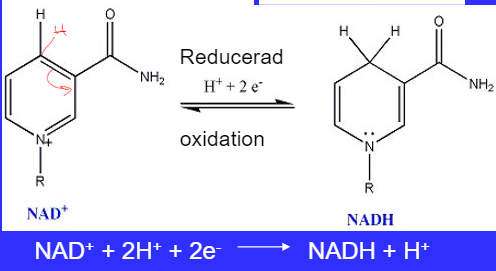
Förstår inte varför det behövs 2 elektroner för då blir det en väteatom som sedan binder till NAD+ och inga protoner blir över, eller?
Eller ska man tänka att en elektron reducerar en väteatom som binder till NAD+, men då skulle den andra elektronen reagera med protonen och produkten skulle istället bli NADH + H.
Men väte är ju en molekyl, så det kanske är så att de två vätejonerna bildar en molekyl när de får de två elektronerna som sedan sönderdelas av NAD+ som tar två elektroner och en Vätejon och det blir en ensam vätejon kvar. Har jag tänkt rätt nu?
Men vad är det som händer inom ringen i strukturformeln, varför försvinner bensenringen och varför reduceras kvävet?
Var har du hittat den bilden? Om du googlar på NAD+ reduction kommer denna reaktionsformeln upp: NAD+ + H+ + 2 e- -> NADH
Från min lärare hehe.
Men antar att din reaktionsformel också är rätt?
NAD+ reduceras och det gör vätet också, tillsammans binder de och bildar NADH eftersom väteatomer inte är stabila.
Det som förvirrar mig nu är mer strukturformeln, reaktionen tror jag jag fått ordning på, dvs om jag tänkte rätt i det första inlägget.
Det som är markerat blått i ditt första inlägg är en förenkling av vad som sker. Och detta kanske är orsaken till att det blivit lite svårt att greppa.
Inom bl.a. citronsyracykeln sker denna typ av reaktion, där ett ämne oxideras och NAD+ samtidigt reduceras. Under reaktionen överförs en hydridjon H- ämnet till NAD+, och NADH bildas. Samtidigt frigörs en proton från detta ämne.
Det är två vätejoner inblandade, men det är två olika vätejoner H- (som reducerar NAD+) samt H+ som "blir över" och lämnas till det omgivande vattnet. Ibland ritas inte protonen som blir över ut, när reaktionen sammanfattas/förenklas ytterligare.
Okej, så hur jag tolka det är felaktigt, att det bildas en vätemolekyl, som bryts upp till en hydridjon och en vätejon, där hydridjonen tas upp av NAD+ och vätejonen blir kvar.
Det som istället sker i den reaktion jag har är att 1 proton tar upp de två elektronerna medan den andra protonen inte reagerar överhuvudtaget. Så egentligen visar fners reaktion de egentliga reaktanterna som faktiskt reagerar medan min visar en extra proton som inte ens är med och reagerar utan simmar runt bara.
Boze skrev:Okej, så hur jag tolka det är felaktigt, att det bildas en vätemolekyl, som bryts upp till en hydridjon och en vätejon, där hydridjonen tas upp av NAD+ och vätejonen blir kvar.
Om du vill se hur det sker är det lättare att titta på en kemisk reaktion, där NAD+ reduceras av ett annat ämne. Din fråga om NAD+ misstänker jag är kopplad till Kemi2 kursens del om ämnesomsättningen, biokemin.
I biokemin gås bl.a. citronsyracyklen igenom, och under denna oxideras organiska ämnen (t.ex. malat) samtidigt som NAD+ reduceras till NADH (detaljer om denna reaktion finns t.ex. på engelskspråkiga Wikipedia).
Det bildas ingen vätgas (den skulle i så fall "bubbla bort" i cellerna, som just en gas). Utan det som sker är att en hydridjon överförs till NAD+, och samtidigt bildas (ofta) en dubbelbindning mellan kol och syre i det organiska ämnet som oxideras. Syreatomen, som tidigare varit en hydroxigrupp får då en positiv laddning, och bryter då bindningen till "sin proton". Och det är då denna proton som "blir över", motsvarande:

Bilden från Wikipedia.


