Laboration Amylas
Hejhej!
Skriver en labbrapport på amylasaktiviteten i olika temperaturer.
Labben gick till så att vi hade olika bägare, och så hade vi i saliv och destillerat vatten i dessa bägare (1:3), sedan hade vi i en blandning av stärkelse och jod.
Jod är ett reagens på stärkelse, och sålänge det finns stärkelse kvar kommer lösningen vara färgad, dvs förskjuten till vänster.
Jag fick dessa resultat:
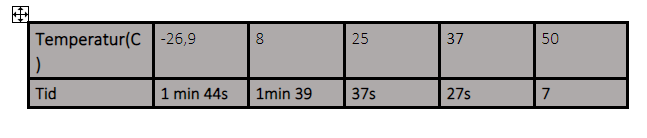
Jag vet inte hur jag ska dra en slutsats utifrån detta riktigt, att amylas är som mest optimal i högre temperaturer? Men det går emot min hypotes där jag skrev att kroppstemperatur var optimalast, då amylas bildas i bukspottskörteln samt att 50 grader c var sämst, då enzymet denaturerats.
Detta är visserligen en sida för ölbryggning så ta det med en nypa salt (och använd kanske inte som källa i din labbrapport), men de har i alla fall en del information om amylas och dess optimala temperatur.
Själva slutsatsen måste du dra utifrån dina resultat, inte utifrån din hypotes. Du kan dock återkoppla till din hypotes i diskussionsdelen och förklara varför din teori inte stämde.
Ja att det var högst aktivitet vid 50°C låter underligt, men kan kanske förklaras utifrån hur experimentet utfördes.
T.ex. om stärkelsen plus buffer fanns som vätska i ett provrör vid rumstemperatur, och amylaset tillsattes, och först efter det sattes provröret i ett 50°C vattenbad - så kommer vätskan i röret värmas upp, och det går så klart snabbare ju varmare vattenbadet är.
Men om röret och dess innehåll redan var 50°C (fick tid att värmas upp i säg 5-10 minuter) innan amylaset tillsattes, så borde "temperaturchocken" fått amylaset att denaturera, och tiden bli mycket längre, kanske till och med så pass lång att inget kunde ske.
Jag misstänker att ni hade stärkelse + buffer i provrör vid rumstemperatur, innan amylaset tillsattes. Annars skulle vätskan ha frusit till is vid -27°C, och ingen reaktion skulle kunna ske vid "den temperaturen" oavsett om amylas tillsattes eller inte.
mag1 skrev:Ja att det var högst aktivitet vid 50°C låter underligt, men kan kanske förklaras utifrån hur experimentet utfördes.
T.ex. om stärkelsen plus buffer fanns som vätska i ett provrör vid rumstemperatur, och amylaset tillsattes, och först efter det sattes provröret i ett 50°C vattenbad - så kommer vätskan i röret värmas upp, och det går så klart snabbare ju varmare vattenbadet är.
Men om röret och dess innehåll redan var 50°C (fick tid att värmas upp i säg 5-10 minuter) innan amylaset tillsattes, så borde "temperaturchocken" fått amylaset att denaturera, och tiden bli mycket längre, kanske till och med så pass lång att inget kunde ske.
Jag misstänker att ni hade stärkelse + buffer i provrör vid rumstemperatur, innan amylaset tillsattes. Annars skulle vätskan ha frusit till is vid -27°C, och ingen reaktion skulle kunna ske vid "den temperaturen" oavsett om amylas tillsattes eller inte.
Det förklarar väldigt mycket, fastän det i sig är lite underligt.
Jag tänker väl mer att 50 grader är 50 grader, oavsett om amylaset får tid att "justera" sig till sin omgivning - ett vattenbad, eller om det är en temperaturchock. En denatureringspunkt är väl en denatureringspunkt oavsett vad omständigheterna var?
aaaa1111 skrev:Det förklarar väldigt mycket, fastän det i sig är lite underligt.
Jag tänker väl mer att 50 grader är 50 grader, oavsett om amylaset får tid att "justera" sig till sin omgivning - ett vattenbad, eller om det är en temperaturchock. En denatureringspunkt är väl en denatureringspunkt oavsett vad omständigheterna var?
Ja i absoluta mått är 50°C, just 50°C. Men precis som vi med en grytlapp/handduk kan hålla i en varm ugnsform, tar det ett litet tag innan våra fingrar bränns. Fingrarna har kroppstemperatur innan, och det tar ett tag för värmen att komma in, och till slut bränna oss (motsvarande denaturera amylaset).
Du har helt rätt i att den temperatur där proteinet denaturerar är en och samma (om allt annat som pH, salt etcetera är konstant). Men enzymets hastighet är beroende av temperaturen, och den maximala hastigheten ligger nära 37°C. Så ju snabbare vätskan når denna temperatur, desto mer substrat kommer att omvandlas per tidenhet.
Du svarade inte på om det var rumstemperatur för provrören, men det antar jag för resten av resonemanget. Samtidigt går det snabbare att värma upp en volym (som amylasvätskan i provrörer), ju högre temperaturen på utsidan är - jämför t.ex. att smälta en isbit i kallt vatten, med att lägga den i rykande varmt te.
Mängden nedbruten stärkelse är ett mått på enzymets aktivitet, ju kortare tid det tar att bryta ner stärkelsen desto snabbare har enzymet arbetat, fler mol stärkelse har då brutits ner per tidsenhet.
Om man illustrerar det grafiskt som i bilden nedan, kommer mängden nedbruten stärkelse beskrivas av arean under de streckade linjerna (som anger enzymets reaktionshastighet). Och om två temperaturer jämförs blir ju arean större i det varmare provet (grön) jämfört med provet i rumstemperatur (blått), för enzymet är mer aktivt.

Men om du börjar vid samma temperatur (rumstemperatur) så kommer det provröret som placeras i 50°C vattenbad att värmas upp (röda linjer), och när temperaturen i provrörets vätska stiger ökar enzymets aktivitet. Det ser då ut som i bilden nedan.
Och ju varmare vattenbadet är desto snabbare stiger värmen i röret, och med den snabbare temperaturökningen blir enzymet mer aktivt - med resultatet att mer substrat kan brytas ner per tidsenhet.
Blir det för varmt, så kommer enzymet att denatureras, men från dina data ser det inte ut som om temperaturen blev så hög att enzymaktiviteten sjönk p.g.a. denaturering av amylaset.


