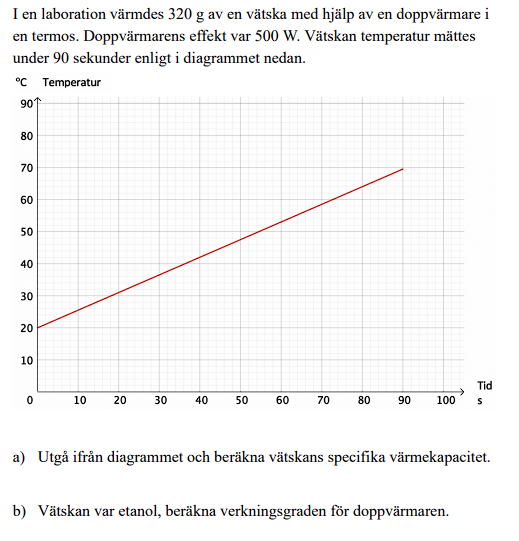
Teckna hur sambandet mellan temperaturhöjningen hos en vätska beror av tillförd energi (ledtråd, använd begreppet värmekapacitet).
Utnyttja sedan att den tillförda energin kan skrivas som tillförd effekt gånger tid.
Jämför sedan med grafen och räta linjens ekvation.
Kommer du vidare?
JohanF skrev:Teckna hur sambandet mellan temperaturhöjningen hos en vätska beror av tillförd energi (ledtråd, använd begreppet värmekapacitet).
Utnyttja sedan att den tillförda energin kan skrivas som tillförd effekt gånger tid.
Jämför sedan med grafen och räta linjens ekvation.
Kommer du vidare?
Så långt har jag typ förstått, men problemet är hur jag översätter grafen till energi på b frågan, jag vet ju hur mycket som sätts in liksom, men jag vet ej hur man kalkylerar värmen till joule, för att sedan få ett förhållande på hur mycket energi som faktiskt går till värme. Jag har som sagt redan gjort a frågan.
Ahh, jag läste för snabbt, såg inte att du redan hade klarat a!
På b gör du precis samma sak som på a, men i a var värmekapaciteten en okänd variabel och effekten en känd konstant (doppvärmarens märkeffekt), som du anpassade till linjen.
På b så har du en känd konstant på värmekapaciteten, medan tillförd effekt är den okända variabeln som du ska anpassa till linjen.
Därefter beräknar du förhållandet tillförd effekt / märkeffekt.
Kommer du vidare?
Nej, jag förstår ej hur jak går ifrån att veta att det är 500 joule/s eller 45000 joule på 90 sekunder, till att veta nyttiga energin.
Tillägg: 22 jan 2023 20:09
Exakt vad är värmekapacitet, kan ha missat förstått djupgående vad det betyder.
Kan du visa hur du räknade ut a, så utgår vi därifrån.
45000=c*0.32*50
Ok. Vilket värde gick du på vätskans värmekapacitet i a-uppgiften?
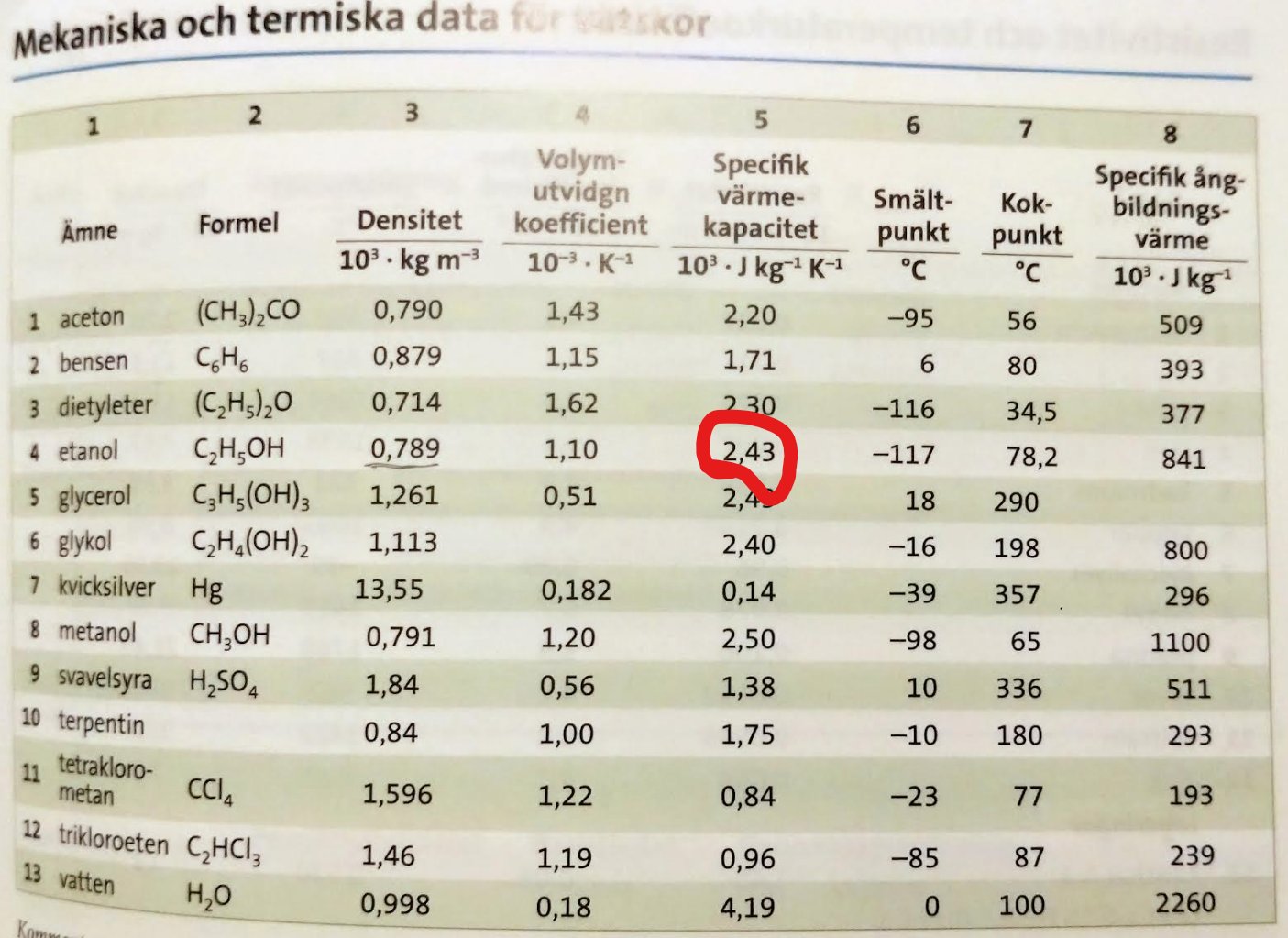
Om du sedan tittar i din tabellsamling, vilken värmekapacitet har etanol?
JohanF skrev:Ok. Vilket värde gick du på vätskans värmekapacitet i a-uppgiften?
Om du sedan tittar i din tabellsamling, vilken värmekapacitet har etanol?
Det är rätt i enligt facit och jag antar att det är ungefär samma. 2800 typ
AlexanderJansson skrev:JohanF skrev:Ok. Vilket värde gick du på vätskans värmekapacitet i a-uppgiften?
Om du sedan tittar i din tabellsamling, vilken värmekapacitet har etanol?
Det är rätt i enligt facit och jag antar att det är ungefär samma. 2800 typ
Ungefär samma duger inte att säga, eftersom det är skillnaden i ditt uträknade värde 2800J/(kgK), och det tabellerade värdet (se foto nedan, 2430J/(kgK)) som gör att du kan räkna ut b.
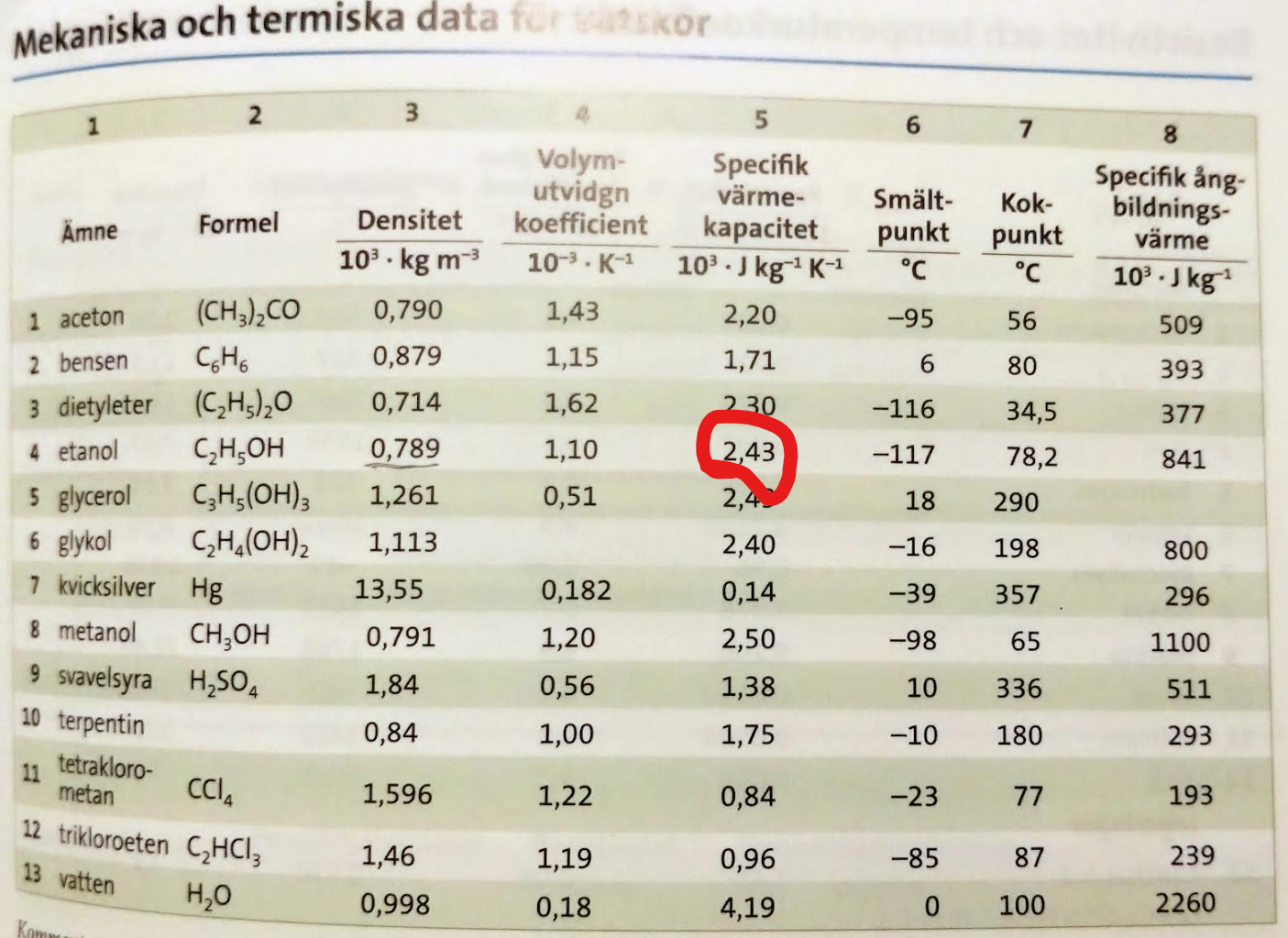
Kan du tänka såhär:
- Värmekapaciteten bestämmer hur mycket energi du måste tillföra för att höja temperaturen på vätskan ett visst antal grader. I ditt fall 50 grader på 90 sekunder.
- Du räknade i a ut att om du tillför 500W*90s energi så höjer du temperaturen med 50 grader _ifall_ värmekapaciteten var 2800J/(kgK). När vi i b vet att värmekapaciteten hos vätskan i själva verket var lägre, så är den enda förklaringen att den experimentellt uppmätta linjen kunde bli som den blev, att den tillförda energin i själva verket var lite lägre än 500W*90s, dvs att en del av doppvärmarens energi inte togs upp av vattnet, utan förlorades någonannanstans.
Så om vi konstruerar en delfråga till b så skulle den kunna lyda: Hur stor energi tillförde doppvärmarenvattnet , om vätskans värmekapacitet var 2430J/(kgK)?
JohanF skrev:AlexanderJansson skrev:JohanF skrev:Ok. Vilket värde gick du på vätskans värmekapacitet i a-uppgiften?
Om du sedan tittar i din tabellsamling, vilken värmekapacitet har etanol?
Det är rätt i enligt facit och jag antar att det är ungefär samma. 2800 typ
Ungefär samma duger inte att säga, eftersom det är skillnaden i ditt uträknade värde 2800J/(kgK), och det tabellerade värdet (se foto nedan, 2430J/(kgK)) som gör att du kan räkna ut b.
Kan du tänka såhär:
- Värmekapaciteten bestämmer hur mycket energi du måste tillföra för att höja temperaturen på vätskan ett visst antal grader. I ditt fall 50 grader på 90 sekunder.
- Du räknade i a ut att om du tillför 500W*90s energi så höjer du temperaturen med 50 grader _ifall_ värmekapaciteten var 2800J/(kgK). När vi i b vet att värmekapaciteten hos vätskan i själva verket var lägre, så är den enda förklaringen att den experimentellt uppmätta linjen kunde bli som den blev, att den tillförda energin i själva verket var lite lägre än 500W*90s, dvs att en del av doppvärmarens energi inte togs upp av vattnet, utan förlorades någonannanstans.
Så om vi konstruerar en delfråga till b så skulle den kunna lyda: Hur stor energi tillförde doppvärmarenvattnet , om vätskans värmekapacitet var 2430J/(kgK)?
2430/2800 alltså
Tillägg: 22 jan 2023 21:04
Nej förlåt mig, vi räknar ut energin först sedan tar vi 38880/45000
Ja precis! Nu verkar du förstå, eller hur?
(och man skulle lika gärna räkna ut förhållandet mellan det tabellerade och det experimentellt uppmätta värmekapaciteterna, och fått samma svar. Men hade du inte motiverat med ord varför du gjorde det, så hade du inte fått full poäng enligt rättningsmallen som du klippte in här ovanför)