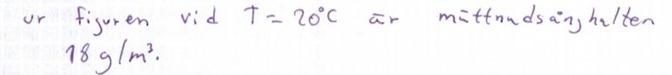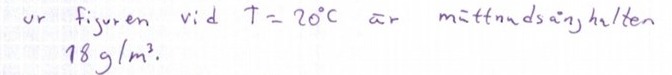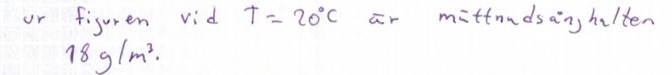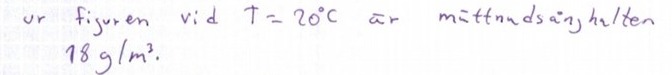Hur många vattenmolekyler finns i luften i rummet?


Hej!
Facit har ett svar på 7.5*10^25 molekyler och jag förstår inte varför mitt svar är felaktigt. Jag var inne på densitet *V =m och sen n=m/M för att få ut substansmängden men var osäker på den vägen så ändrade mig till ideala gaslagen. Sen visste jag inte hur jag skulle ta hänsyn till relativa luftfuktigheten som anges där.
destiny99 skrev:
Facit har ett svar på 7.5*10^25 molekyler och jag förstår inte varför mitt svar är felaktigt. Jag var inne på densitet *V =m och sen n=m/M för att få ut substansmängden men var osäker på den vägen så ändrade mig till ideala gaslagen. Sen visste jag inte hur jag skulle ta hänsyn till relativa luftfuktigheten som anges där.
Du får fel för att du tar fel tryck. Det ska vara ångans partialtryck istället.
Men det enklaste sättet att räkna ut uppgiften är att se att mättnadsångtrycket motsvarar 1 mol/m3.
Pieter Kuiper skrev:destiny99 skrev:
Facit har ett svar på 7.5*10^25 molekyler och jag förstår inte varför mitt svar är felaktigt. Jag var inne på densitet *V =m och sen n=m/M för att få ut substansmängden men var osäker på den vägen så ändrade mig till ideala gaslagen. Sen visste jag inte hur jag skulle ta hänsyn till relativa luftfuktigheten som anges där.
Du får fel för att du tar fel tryck. Det ska vara ångans partialtryck istället.
Men det enklaste sättet att räkna ut uppgiften är att se att mättnadsångtrycket motsvarar 1 mol/m3.
Vad är ångans partialtryck då? Är det givet i uppgiften? I formelbladet står det 1 atm=10^5 Pa.
destiny99 skrev:Pieter Kuiper skrev:destiny99 skrev:
Facit har ett svar på 7.5*10^25 molekyler och jag förstår inte varför mitt svar är felaktigt. Jag var inne på densitet *V =m och sen n=m/M för att få ut substansmängden men var osäker på den vägen så ändrade mig till ideala gaslagen. Sen visste jag inte hur jag skulle ta hänsyn till relativa luftfuktigheten som anges där.
Du får fel för att du tar fel tryck. Det ska vara ångans partialtryck istället.
Men det enklaste sättet att räkna ut uppgiften är att se att mättnadsångtrycket motsvarar 1 mol/m3.Vad är ångans partialtryck då? Är det givet i uppgiften? I formelbladet står det 1 atm=10^5 Pa.
Den skulle man behöva räkna ut här.
I andra uppgifter är kanske den här grafen given: mättnadsångtryck som funktion av temperatur.
Pieter Kuiper skrev:destiny99 skrev:Pieter Kuiper skrev:destiny99 skrev:
Facit har ett svar på 7.5*10^25 molekyler och jag förstår inte varför mitt svar är felaktigt. Jag var inne på densitet *V =m och sen n=m/M för att få ut substansmängden men var osäker på den vägen så ändrade mig till ideala gaslagen. Sen visste jag inte hur jag skulle ta hänsyn till relativa luftfuktigheten som anges där.
Du får fel för att du tar fel tryck. Det ska vara ångans partialtryck istället.
Men det enklaste sättet att räkna ut uppgiften är att se att mättnadsångtrycket motsvarar 1 mol/m3.Vad är ångans partialtryck då? Är det givet i uppgiften? I formelbladet står det 1 atm=10^5 Pa.
Den skulle man behöva räkna ut här.
I andra uppgifter är kanske den här grafen given: mättnadsångtryck som funktion av temperatur.
Hur räknar man ut partialtryck hos ångan då? Man kan använda PV=nRT. Men vi har ju given i g/m^3 så jag antar man ska använda rå*V=m och sen n=rå*V/M(H2O)
destiny99 skrev:
Hur räknar man ut partialtryck hos ångan då?
Uppgiften var att beräkna antalet vattenmolekyler.
Given är en graf av mängden vatten som funktion av temperatur i 100 % mättad luft.
Man läser av att det är 18 gram per kubikmeter.
Det är en mol per kubikmeter.
Pieter Kuiper skrev:destiny99 skrev:
Hur räknar man ut partialtryck hos ångan då?Uppgiften var att beräkna antalet vattenmolekyler.
Given är en graf av mängden vatten som funktion av temperatur i 100 % mättad luft.
Man läser av att det är 18 gram per kubikmeter.
Det är en mol per kubikmeter.
Ja precis jag läste också av 18 g/m^3 vid T=20 grader. Dock är jag inte med på hur det är en mol /m^3?
destiny99 skrev:Pieter Kuiper skrev:destiny99 skrev:
Hur räknar man ut partialtryck hos ångan då?Uppgiften var att beräkna antalet vattenmolekyler.
Given är en graf av mängden vatten som funktion av temperatur i 100 % mättad luft.
Man läser av att det är 18 gram per kubikmeter.
Det är en mol per kubikmeter.Ja precis jag läste också av 18 g/m^3 . Dock är jag inte med på hur det är en mol /m^3?
Hur stor är vattnets molekylvikt?
Pieter Kuiper skrev:destiny99 skrev:Pieter Kuiper skrev:destiny99 skrev:
Hur räknar man ut partialtryck hos ångan då?Uppgiften var att beräkna antalet vattenmolekyler.
Given är en graf av mängden vatten som funktion av temperatur i 100 % mättad luft.
Man läser av att det är 18 gram per kubikmeter.
Det är en mol per kubikmeter.Ja precis jag läste också av 18 g/m^3 . Dock är jag inte med på hur det är en mol /m^3?
Hur stor är vattnets molekylvikt?
18 g/mol. Juste så 18 g/cm^3 är 100% luftfuktighet av mättnadånghalt medan vi har bara fått givet 50% så vi behöver få ut densitet vid den delen som är 18 g/cm^3*0.5 .