elektronformel för kväveflourid
Hur ritar man ut elektronfomeln för kvävefluorid?
Jag vet att kväve har 5 valenselektroner och fluor 7 valenselektroner
Hur ska jag veta hur många fluor och hur många kväve som finns i föreningen?
Hej,
Här är en beskrivande bild. Kan du klura ut hur man ritar den?
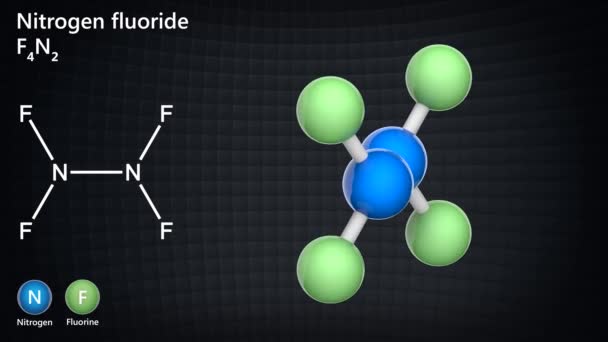
Mesopotamia skrev:Hej,
Här är en beskrivande bild. Kan du klura ut hur man ritar den?
kväve binder till varandra med en trippelbindning och fluor binder till kväve med enkelbindningar vilket gör att också de får åtta valens elektroner. Men hur ska jag från början fatta hur många av varje som behövs?
När jag googlar kvävefluorid får jag förövrigt upp formeln NF3, hur går det ihop? det står kvävetrifluorid men att den också kan heta kvävefluorid.
fjälllämmel3301 skrev:Hur ritar man ut elektronfomeln för kvävefluorid?
Jag vet att kväve har 5 valenselektroner och fluor 7 valenselektroner
Hur ska jag veta hur många fluor och hur många kväve som finns i föreningen?
Fluor behöver låna en elektron från en annan atom för att få ädelgasstruktur. Kväve behöver låna tre elektroner från andra atomer för att få ädelgasstruktur. Varje kväveatom har alltså tre bindningar, och varje fluoratom en. Får du ihop det då?



