Elektronen runt en väteatom
Hej!
Min fråga är: har elektronen i väteatomen positiv eller negativ potentiell energi när den snurrar i bana runt protonerna?
Jag tänker att så länge banan har konstant radie så kommer elektronernas potentiell energi inte ändras, för då har de samma avstånd från protonerna. och för att utföra arbete måste F (qE) vara parallell med s. Vilket elektronens bana inte är.
Men något känns fel i mitt resonemang. Tänker jag rätt?
Tack i förhand!
Man brukar tala om vilken energi elektronen har i förhållade till dess ursprungliga position, ursprungliga skal. Den kan vara mindre eller större, dock är energin som den har aldrig mindre än 0.
F=ma eller W=Fs tror jag inte fungerar på en så liten skala.
Du kommer få svar på dina frågor när din lärare har gått igenom allt. Om du vill kan du läsa i förväg i boken, där finns svaren du letar efter.
nur yusuf skrev:Hej!
Min fråga är: har elektronen i väteatomen positiv eller negativ potentiell energi när den snurrar i bana runt protonerna?
Jag tänker att så länge banan har konstant radie så kommer elektronernas potentiell energi inte ändras, för då har de samma avstånd från protonerna. och för att utföra arbete måste F (qE) vara parallell med s. Vilket elektronens bana inte är.
Men något känns fel i mitt resonemang. Tänker jag rätt?
Tack i förhand!
Nja, skulle inte säga att du tänker fel.
Men ja, energin hos elektroner runt en väteatom är kvantiserad. Använder vi Bohrmodellen där energinivån för en elektron beror på kvanttalet n så kan du räkna ut energinivån med följande formel:
OBS: I bohrmodellen så är elektronernas bana inte cirklar utan vågor. Hade elektronernas bana varit cirklar såsom i Rutherfordmodellen så hade det skett en konstant acceleration -> synkrotronljus sänds ut, elektronen tappar energi -> atomen kollapsar och vårt universum som det är hade inte existerat. Bohrmodellen är inte heller helt korrekt, en ännu korrektare modell beskrivs av Schrödingerekvationen. Men också den är en approximation
Så ja, elektronen runt en väteatom har positiv potentiell energi. Precis som Qetsiyah säger brukar man dock prata om energin som elektronen har i förhållande till sitt utgångskvanttillstånd. När en elektron hoppar mellan olika kvanttillstånd kommer det antingen absorberas eller sändas ut en foton med energi ekvivalent till den mellan två olika kvanttillstånd. Då är det smidigt men måhända slarvigt att säga att elektronen har negativ potentiell energi.
Man brukar demonstrera det visuellt genom att låta energinivån vid
motsvara E=0 eV
Då kommer energinivån vid n=1 ha negativt tecken i förhållande till E=0 eV vid oändligt stort n.
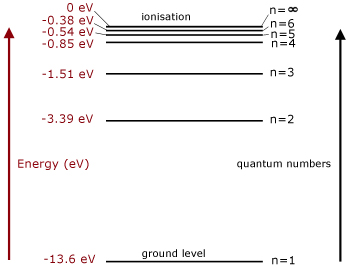
Ovan ser du en visuell representation där man av enkelhets skull säger att elektronernas potentiella energi är negativ. Vilket de egentligen inte är men i förhållande till n=oändlighetens energinivå så är de det.
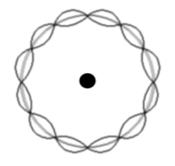
Visualisering av Bohrmodellen av en elektron runt en vätekärna.
Källa: http://www.a-levelphysicstutor.com/quantphys-energy-levels.php
Läs för övrigt ovanstående länk om du tycker jag förklarar för dåligt (vilket jag säkert gör).
Du förklarade så bra! :)
Jag tänkte inte på det här resonemanget men nu förstår jag så tack så mycket för hjälpen!


