8
svar
60
visningar
Bayan Ali behöver inte mer hjälp
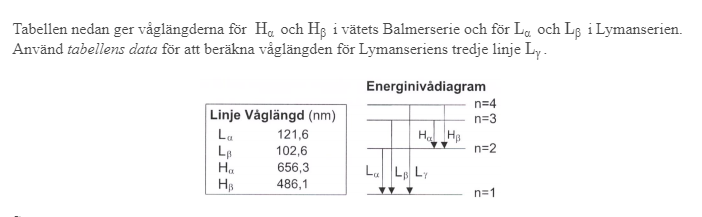
Bestäm våglängden
E = hc/lambda
E = -B/n^2
Jag försökte bestämma B för de olika linjerna och får dessa värden, kommer dock inte vidare.
B för La = 6.54*10^-18
B för Lb = 1.74*10^-18
B för Ha = 2.73*10^-18
B för Hb = 6.54*10^-18
Använd Rydberg-Ritz kombinationsprincipen.
Vad är en kombination av?
Jag känner inte till denna princip. Finns det ett annat sätt att lösa uppgiften på, om inte vad handlar principen om?
Du kan ju se i energinivådiagrammet vad är en kombination av.
HB och La alltså 607.7
Bayan Ali skrev:HB och La
Ja.
Så addera fotonenergierna.
2.05*10^-18J
Och svara på uppgiftens fråga.
Visa spoiler
(förkorta med hc)
(Rydberg-Ritz)
Så det blir 97nm?


