balansre
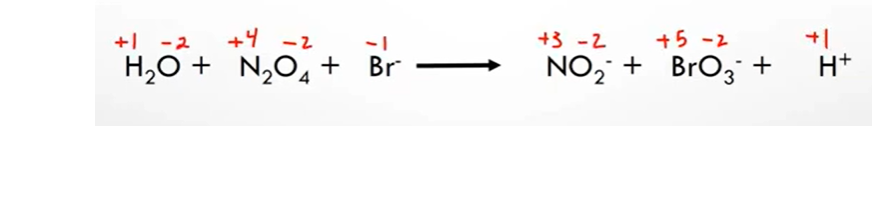
från en extra uppgift som min lärare gett ut, man ska balansera mha oxidationstalmetoden. (jag vet att man skriver med romerska siffror men det är för enkelhetensskull)
N --> 4 till 3 (1 steg)
Br --> -1 till 5 (6 steg)
sedan tänker jag att multiplicerar in (6) till alla ställen där N finns, tänker jag rätt? skulle någon kunna vägleda mig vidare..
Nja, du ska inte multiplicera in något. Försök göra som i mitt exempel här:
Teraeagle skrev:Nja, du ska inte multiplicera in något. Försök göra som i mitt exempel här:
vi har inte riktigt gått igenom allt och vad det gäller sura respektive basiska lösningar, men jag kollade igenom det du hade skrivit och det förenklade.
men en fråga som dykt upp är hur man kan separera sammansatta joner? har sett saltsyra främst men är rätt säker på att det går på fler, men förstår inte hur, kommer inte ämnena då att ändras?
exempel på det jag menar:

Salpetersyra är inte en sammansatt jon. Det är en stark syra som i vattenlösning är fullständigt uppdelad i vätejoner (oxoniumjoner) och nitratjoner. Det finns inga HNO3-molekyler i en vattenlösning, därför skriver man som man gör.
Teraeagle skrev:Salpetersyra är inte en sammansatt jon. Det är en stark syra som i vattenlösning är fullständigt uppdelad i vätejoner (oxoniumjoner) och nitratjoner. Det finns inga HNO3-molekyler i en vattenlösning, därför skriver man som man gör.
då är jag med!
hur vet jag vad slutprodukterna blir i en reaktion?
vi säger att jag bara hade fått vänsterledet angivet, hur vet jag att slutreaktionen på högerledet kommer att se ut så? (om det bildas nya ämnen, enskilda atomer m.m)
Inom gymnasiekemin får du alltid veta vad som bildas, såvida det inte står något som ”fullständig förbränning”. Då ska man känna till att det innebär att produkterna blir koldioxid och vatten.
I verkligheten kan man simulera en reaktion, dvs man tar in en massa termodynamiska data och räknar fram vilka produkter som borde bildas. Eller så gör man experiment och tar reda på det.
Teraeagle skrev:Inom gymnasiekemin får du alltid veta vad som bildas, såvida det inte står något som ”fullständig förbränning”. Då ska man känna till att det innebär att produkterna blir koldioxid och vatten.
I verkligheten kan man simulera en reaktion, dvs man tar in en massa termodynamiska data och räknar fram vilka produkter som borde bildas. Eller så gör man experiment och tar reda på det.
jag har stött på några uppgifter där man förväntas kunna slutprodukterna
exempelvis
Slutför och balansera reaktionsformlerna i de fall reaktion sker (du måste ta hjälp av den elektrokemiska spänningsserien i din lärobok):
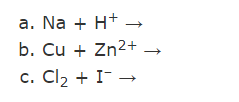
b frågan sker det ingenting.
men a+c? (a frågan vet jag bildar vätgas dock men är osäker när det gäller att skriva ut vad som bildas, speciellt c frågan)
hur "får man fram det" och hur tänker man?
a) och b) kan du få fram från elektrokemiska spänningsserien och kunskap om väteutdrivande metaller.
c) kan du lösa utifrån kunskaper om halogenernas reaktiviter. Halogenerna blir mindre oxiderande ju längre ner i gruppen man kommer. Fluor är t.ex. mer oxiderande än klor, så fluor kan oxidera kloridjoner men klor kan inte oxidera fluoridjoner.
Teraeagle skrev:a) och b) kan du få fram från elektrokemiska spänningsserien och kunskap om väteutdrivande metaller.
c) kan du lösa utifrån kunskaper om halogenernas reaktiviter. Halogenerna blir mindre oxiderande ju längre ner i gruppen man kommer. Fluor är t.ex. mer oxiderande än klor, så fluor kan oxidera kloridjoner men klor kan inte oxidera fluoridjoner.
ja, det är jag med på, tack
men jag blir osäker om vad som bildas, alltså om det exempelvis blir (på c) bara I eller I- (gas, flytande, fast m.m)(nu var detta ett dåligt exempel) men på vissa frågor blir jag osäker gällande vad det blir i slutet
eller är hela konceptet egentligen att avgöra om vilka som blir reducerade och oxiderade?
naturnatur1 skrev:Teraeagle skrev:Salpetersyra är inte en sammansatt jon. Det är en stark syra som i vattenlösning är fullständigt uppdelad i vätejoner (oxoniumjoner) och nitratjoner. Det finns inga HNO3-molekyler i en vattenlösning, därför skriver man som man gör.
då är jag med!
hur vet jag vad slutprodukterna blir i en reaktion?
vi säger att jag bara hade fått vänsterledet angivet, hur vet jag att slutreaktionen på högerledet kommer att se ut så? (om det bildas nya ämnen, enskilda atomer m.m)
För att återkoppla lite till detta:
Se detta som överkurs, men när man simulerar ett system så får man ofta ut ett Pourbaix-diagram som visar vilka species som är mest stabila vid en viss redoxpotential och ett visst pH. Såhär kan ett diagram för vismut, svavel och vatten se ut:
 För att få Bi3+(aq) måste man befinna sig i området markerat med Bi2(SO4)3 dvs pH måste vara lägre än typ 3,5 och redoxpotentialen högre än 0,3 V. Redoxpotential och pH kan man justera genom att anpassa koncentrationen av salpetersyra.
För att få Bi3+(aq) måste man befinna sig i området markerat med Bi2(SO4)3 dvs pH måste vara lägre än typ 3,5 och redoxpotentialen högre än 0,3 V. Redoxpotential och pH kan man justera genom att anpassa koncentrationen av salpetersyra.
naturnatur1 skrev:Teraeagle skrev:a) och b) kan du få fram från elektrokemiska spänningsserien och kunskap om väteutdrivande metaller.
c) kan du lösa utifrån kunskaper om halogenernas reaktiviter. Halogenerna blir mindre oxiderande ju längre ner i gruppen man kommer. Fluor är t.ex. mer oxiderande än klor, så fluor kan oxidera kloridjoner men klor kan inte oxidera fluoridjoner.
ja, det är jag med på, tack
men jag blir osäker om vad som bildas, alltså om det exempelvis blir (på c) bara I eller I- (nu var detta ett dåligt exempel) men på vissa frågor blir jag osäker gällande vad det blir i slutet
eller är hela konceptet egentligen att avgöra om vilka som blir reducerade och oxiderade?
Halogener existerar aldrig som fria atomer, de finns alltid i par. Alltså blir produkten I2 och inte I.
Teraeagle skrev:naturnatur1 skrev:Teraeagle skrev:a) och b) kan du få fram från elektrokemiska spänningsserien och kunskap om väteutdrivande metaller.
c) kan du lösa utifrån kunskaper om halogenernas reaktiviter. Halogenerna blir mindre oxiderande ju längre ner i gruppen man kommer. Fluor är t.ex. mer oxiderande än klor, så fluor kan oxidera kloridjoner men klor kan inte oxidera fluoridjoner.
ja, det är jag med på, tack
men jag blir osäker om vad som bildas, alltså om det exempelvis blir (på c) bara I eller I- (nu var detta ett dåligt exempel) men på vissa frågor blir jag osäker gällande vad det blir i slutet
eller är hela konceptet egentligen att avgöra om vilka som blir reducerade och oxiderade?
Halogener existerar aldrig som fria atomer, de finns alltid i par. Alltså blir produkten I2 och inte I.
oj ja det är klart, ursäkta!
men jag förstår fortfarande inte hur man ska tänka för att avgöra vilka ämnen det blir i slutprodukt och i vilket aggregationsstillstånd de blir i efter reaktionen :c
(alltså utöver elektrokemiska spänningsserien och "reglerna" för halogener)
Ja alltså det finns ju inte ett sätt, utan det varierar i uppgift till uppgift hur du måste tänka. Du måste kombinera saker som du har lärt dig. Jod är t.ex. ett fast ämne vid rumstemperatur, men kan bilda jodånga vid höga temperaturer. Måste du veta det utantill? Nej, men det underlättar och du kommer med tiden lära dig det. Du kan även se aggregationstillståndet vid rumstemperatur om du kollar i ett periodiskt system (som garanterat finns i ditt kursmaterial). Smält- och kokpunkter finns säkert i din formelsamling, annars kan du slå upp ämnet på Wikipedia så finns det angivet där.
Teraeagle skrev:Ja alltså det finns ju inte ett sätt, utan det varierar i uppgift till uppgift hur du måste tänka. Du måste kombinera saker som du har lärt dig. Jod är t.ex. ett fast ämne vid rumstemperatur, men kan bilda jodånga vid höga temperaturer. Måste du veta det utantill? Nej, men det underlättar och du kommer med tiden lära dig det. Du kan även se aggregationstillståndet vid rumstemperatur om du kollar i ett periodiskt system (som garanterat finns i ditt kursmaterial). Smält- och kokpunkter finns säkert i din formelsamling, annars kan du slå upp ämnet på Wikipedia så finns det angivet där.
tänkte om det fanns ett sätt utan hjälpmedel (då man inte har hjälpmedel tillgängligt) självklart har man dock formelsamling m.m.
men jag förstår hur du menar och tusen tack för hjälpen
Tja, du kan ju memorera en massa saker men det behöver du inte eftersom du kommer få tillräckligt med hjälpmedel på t.ex. ett prov. Se det lite som att lära sig ett språk. Hur vet man varför ord stavas och böjs på vissa sätt? Man skriver och pratar språket så mycket att man till slut kan det utantill. Det finns ordböcker och skrivregler, men om man alltid behövde titta på dem skulle det ta lång tid att uttrycka sig.
Det fungerar på samma sätt inom kemin, sysslar man med det tillräckligt ofta kommer man att lära sig saker utantill.
Teraeagle skrev:Tja, du kan ju memorera en massa saker men det behöver du inte eftersom du kommer få tillräckligt med hjälpmedel på t.ex. ett prov. Se det lite som att lära sig ett språk. Hur vet man varför ord stavas och böjs på vissa sätt? Man skriver och pratar språket så mycket att man till slut kan det utantill. Det finns ordböcker och skrivregler, men om man alltid behövde titta på dem skulle det ta lång tid att uttrycka sig.
Det fungerar på samma sätt inom kemin, sysslar man med det tillräckligt ofta kommer man att lära sig saker utantill.
ja, tack snälla(:


