Är det rätt tänkt angående Alanins stereoisomer?
Jag sitter med en uppgift där man ska plocka fram alanins spegelbildsisomerer. Jag är lite osäker på hur man ska tänka men jag har gjort ett försök enligt bilden nedan:

Är det rätt tänkt att spegelbildsisomeren erhålls genom att "byta plats" på bindningarna från det asymmetriska kolet som går in respektive ut ur planet? Det verkar med mitt enkla förstånd då som om strukturen borde ändras.
Jag vet inte om det var det du menade, men dessa två är stereoisomerer:

Jo, det var det jag menade! Vanligtivs brukar man bara "spegelvända" molekylen (när man inte ritar molekylen med dess 3D-struktur, det var därför jag vred den i ritningen nedan).
En halvt orelaterad fråga också:
Jag bara gissade att väteatomen på det asymmetriska kolet skulle gå in i planet (i min molekyl längst upp) eftersom ingen annan bindning verkade göra det och kolet ju är sp3-hybridiserat. Men hade det funnits något sätt att lista ut det bara med vetskapen att Alanin är 2-aminopropansyra?
sp3-hybridisering innebär att man har fyra elektrontäta områden som enligt VSEPR då bildar en tetraeder. Två av dessa områden binder i ”huvudkedjan”. Resterande två till väteatomen och sidokedjan. Dessa två områden pekar in i respektive ut från pappret om huvudkedjan ligger i papprets plan. Beroende på till vilken av de två orbitalerna vätet binder får man de två isomererna.
Dessa två områden pekar in i respektive ut från pappret om huvudkedjan ligger i papprets plan.
Ja okej. Kan man anta att huvudkedjan alltid ligger i samma plan? Alltså att den inte helt plötsligt vid någon kolatom böjer sig gentemot de andra kolatomerna?
Det spelar inte så stor roll eftersom man har fri rotation runt dessa bindningar. Jag tycker det är enklast att tänka att hela den kedjan ligger i papprets plan för att sen klura ut vinklarna för övriga atomer och kedjor. Rent principiellt kan du rita vätet och sidokedjan i papprets plan och huvudkedjan framför/bakom planet.
Jag förstår inte riktigt hur det är relevant att kolatomerna i huvudkedjan har fri rotation kring sina bindningar. Jag kan ta ett exempel för att förtydliga min fråga. Skulle följande molekyl vara möjlig?:
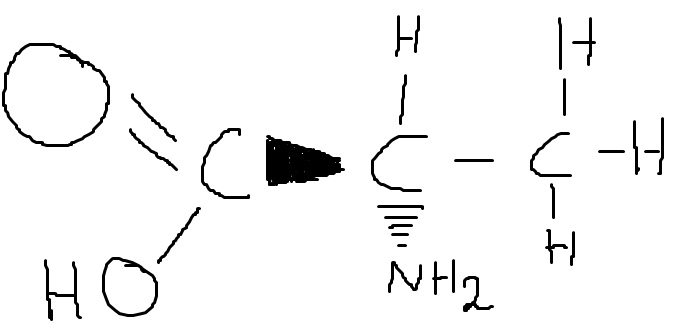
Men blir inte det en helt annan molekyl egenskapsmässigt jämfört med den ursprungliga i frågan?:
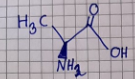
Molekylen i inlägg #8 är samma som den du döpte till "möjlig isomer" i första inlägget. Det var det jag menade med fri rotation, för molekylen i inlägg #8 kan du vrida 90 grader "in mot skärmen" nedifrån och upp, sedan 180 grader höger-vänster så att du får "möjlig isomer"-molekylen..
Okej. Jag ska bygga molekylen själv för att övertyga mig själv om det (även om jag kan föreställa mig det du beskriver).
Kan man ha som allmän strategi att man alltid ritar in kolen i huvudkedjan i samma plan?
Ja det kan man, åtminstone när det är enklare föreningar.
Vad skulle du klassa som en "enklare" förening? Jag var på en lite populärvetenskaplig föreläsning häromveckan och föreläsaren pratade om att vissa i naturen förekommande molekyler var för komplexa för att syntetisera, och att man kunde gå på antalet sterogena centra för att avgöra "hur" komplex molekylen är. Är det något liknande du menar?
Om man har flera dubbel- eller trippelbindningar kan det ibland vara klurigt att föreställa sig hur kedjan går att veckla ut, åtminstone tycker jag det. Om man bara har ett fåtal atomer i en kedja med enkelbindningar går den alltid att veckla ut så atomerna i kedjan ligger i samma plan.



